


















公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
公司地址:新疆和田洛浦县杭桂路232号
摘 要:为完善和提升安中通便胶囊的质量标准,文章以薄层色谱法鉴别方中姜厚朴及肉苁蓉;以高效液相色谱(high performance liquid chromatography,HPLC)法测定君药中大黄素及大黄酚的质量,并以现行版中国药典方法进行微生物限度检查验证试验。试验结果表明:姜厚朴及肉苁蓉的薄层特征斑点清晰,分离度好,阴性无干扰;安中通便胶囊中大黄素、大黄酚质量浓度线性范围分别为0.006~0.144mg/mL(r=0.999 7)、0.018~0.420mg/mL(r=0.999 6),大黄素平均加样回收率为98.95%,相对标准偏差(relativestandard deviation,RSD)为0.97%;大黄酚的平均加样回收率为96.77%,RSD为0.84%。安中通便胶囊各菌的回收率在0.5~2.0区间。该试验新增的薄层鉴别、含量测定及微生物限度检查方法操作简便、专属性强,重复性好,可为进一步提升该制剂的质量标准提供依据。
关键词:安中通便胶囊;薄层色谱鉴别;微生物限度;含量测定
安中通便胶囊(批准文号:皖药制字20080003)是安徽中医药大学第一附属医院的特色中药制剂品种,源于本院肛肠科,临床应用近20年,由大黄、麸炒枳实、炒火麻仁、炒白芍、炒瓜蒌子、姜厚朴、肉苁蓉七味中药组成,诸药合用,具泻热通腑、润肠通便之功效,用于肠道热结腑气不通型、气机郁滞型及阴血亏虚兼燥热型便秘。该制剂临床疗效确切,广受患者好评[1-2]。本试验在前期研究的基础上[3],以薄层色谱法(thin layerchromatography,TLC)对姜厚朴、肉苁蓉进行定性鉴别;采用现行版药典方法进行微生物限度检查验证试验,以高效液相色谱法(high performance liquid chromatography,HPLC)对君药大黄的主要成分(大黄素、大黄酚)进行测定,为进一步提升该制剂的质量标准提供依据,从而保证安中通便胶囊在临床应用的有效性和安全性。
1 仪器与试药
1260型高效液相色谱仪(含G4212B型的二极管阵列检测器、G1311C型的四元泵和G1329B型的自动进样器)(Agilent公司);CAMAG 荧光灯、定量毛细管(瑞士CAMAG公司);薄层硅胶G板和硅胶GF254薄层板(青岛海洋化工集团);聚酰胺薄膜(浙江省台州市路桥四甲生化塑料厂);BP211D型电子天平(德国赛多利斯公司);101A-S1数显电热鼓风干燥箱(上海浦东荣丰科学仪器有限公司);SK3200H 超声波清洗器(天津天有利科技有限公司);BSC-250型恒温恒湿培养箱和YXQ-50SII型立式压力蒸汽灭菌器(上海博迅实业有限公司);BSC-1100ⅡB2-X型生物安全柜(济南鑫贝西生物技术有限公司)等。大黄素对照品(批号110756-201512)、大黄酚对照品(批号110796-201520)、厚朴对照药材(批号121285-201303)、肉苁蓉对照药材(批号
121101-200402),均购自中国食品药品检定研究院;安中通便胶囊(批号20180310、20180506、20180810、20181012、20181221、20190108)由安徽中医药大学第一附属医院制剂中心提供;大黄、姜厚朴等药材饮片,由安徽中医药大学第一附属医院中草药房提供;水为屈臣氏水;甲醇为色谱纯;其余试剂均为分析纯。
胰酪胨大豆琼脂培养基(批号1350025-201803)、沙氏葡萄糖琼脂对照培养基(批号135013-1802)、胰酪大豆胨液体培养基(批号135025-201802)、麦康凯液体培养基(批号135030-201801)、麦康凯琼脂培养基(批号135009-201803),均购于中国食品药品检定研究院。金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、白色念珠菌、枯草芽孢杆菌,均由中国医学细菌保藏中心提供;黑曲霉由中检院提供,本实验使用的为三代菌种。
2 方法与结果
2.1 薄层鉴别
2.1.1 姜厚朴
取安中通便胶囊内容物3g,加甲醇10mL置具塞锥形瓶中,密塞,充分振摇30min,过滤,蒸干滤液,加甲醇5mL溶解,即为供试品溶液。取厚朴对照药材1g,同法制成对照药材溶液。称厚朴酚对照品1mg,加甲醇制成每1mL含1mg的溶液,即为对照品溶液。按安中通便胶囊制备工艺制成缺厚朴的阴性样品,并按供试品溶液制备方法,制得缺姜厚朴的阴性对照溶液[4-6]。按薄层色谱法[现行版药典(四部)通则(0502)]试验,吸取供试溶液(5μL)、厚朴酚对照品溶液(5μL)和厚朴对照药材(2μL),点在同一块GF254薄层板上,以甲苯-甲醇为展开剂(体积比17∶1),上行展开,拿出,室温晾干,再喷以香草醛硫酸溶液(1%),加热(105℃)至斑点明显。置UV灯下检视(254nm)。安中通便胶囊供试品色谱中,在与厚朴对照药材、厚朴酚对照品色谱相应的位置上,显现出相同的暗斑点,且缺厚朴的阴性对照无此暗斑点,如图1所示。
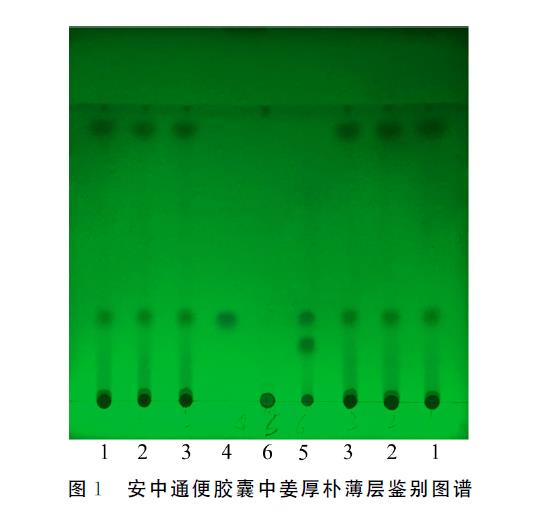
图1 中,1~3 为供试品,批号分别为20180310、20180810、20181012;4为厚朴酚对照品,批号为110729-201513;5为厚朴对照药材,批号为121285-201303;6为缺姜厚朴的安中通便胶囊阴性对照。
2.1.2 肉苁蓉
取安中通便胶囊内容物3g,加甲醇10mL,置锥形瓶中,密塞后,振摇15min,过滤后蒸干,加甲醇5mL溶解,即为供试品溶液。称肉苁蓉对照药材1g,相同方法制成对照药材溶液。按安中通便胶囊制备工艺制备缺肉苁蓉的阴性制剂,并按上述安中通便胶囊供试品溶液制备方法,同法制得安中通便胶囊缺肉苁蓉的阴性对照溶液。按现行版《中国药典(四部)》通则(0502)薄层色谱法试验,吸取供试溶液(1μL)和对照药材(1μL),点在同一聚酰胺薄膜上,以甲醇-醋酸-水展开剂(体积比2∶1∶7)上行展开,拿出,室温晾干,置UV灯下检视(254nm)。安中通便胶囊供试品色谱中,在与肉苁蓉对照药材色谱相应的位置上显示相同的蓝斑点,而缺肉苁蓉的阴性对照无此斑点,如图2所示。
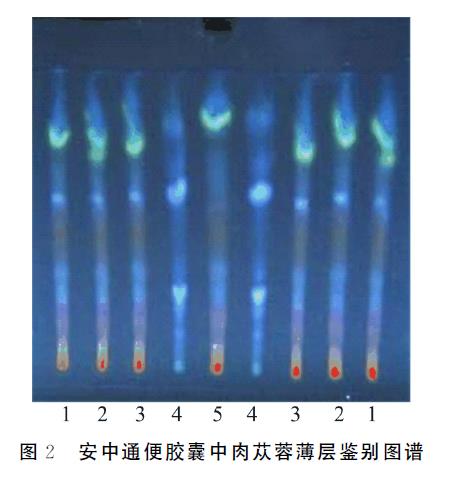
图2 中,1~3 为供试品,批号分别为20180310、20180810、20181012;4为肉苁蓉对照药材,批号为121101-201402;5为缺肉苁蓉的安中通便胶囊阴性对照。
2.2 微生物限度检查
2.2.1 菌液和供试液制备
按现行版药典四部1105及1106方法制备菌液。取本品内容物10g,加入pH 值为7.0无菌氯化钠-蛋白胨缓冲液使总体积为100mL,混匀,得供试液(1∶10)。
2.2.2 菌总数计数方法适用性实验
试验组。取5份供试液,每份10mL。取其中3份供试液,分别加入上述不大于10 000cfu/mL的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的菌液0.1mL,混匀(每mL供试液中的含菌量≤100cfu),各取1mL加入平皿中,倾注不超过45 ℃的胰酪大豆胨琼脂培养基20 mL,35℃培养3d,逐日观察结果。取另外2份供试液,分别加入上述不大于10 000cfu/mL的黑曲霉菌、白色念珠菌液0.1mL,混匀(每mL供试液中的含菌量≤100cfu),各取1mL加入平皿中,倾注不超过45 ℃ 的胰酪大豆胨琼脂培养基20mL,35℃培养5d,另分别取1mL加入平皿中,倾注不超过45℃的沙氏葡萄糖琼脂培养基20mL,25℃培养5d,逐日观察结果。菌液对照组见菌液的制备。供试品对照组取1∶10的供试液,按通则1105中供试品检查方法进行[7]。计算加菌回收率,结果见表1所列。
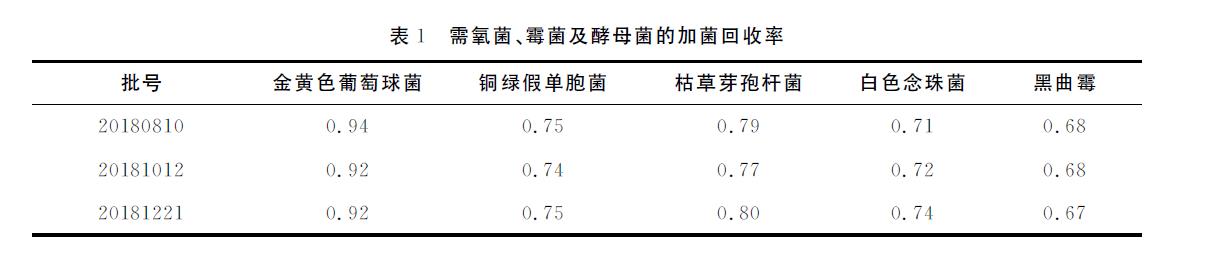
从表1可以看出,安中通便胶囊回收率都在0.5~2.0区间内,符合现行版药典要求,说明该法可用来测定安中通便胶囊中需氧菌总数、霉菌及酵母菌总数。
2.2.3 大肠埃希菌检查方法适用性实验
试验组。取10mL供试液(1∶10)及1mL
2.2.1节的菌液(≤100cfu/mL大肠埃希菌),都加至100mL胰酪大豆胨液体培养基中,混匀,培养24h(35℃),按通则1106相应的控制菌的检查法检查。阴性对照组。以等体积的胰酪大豆胨液体培养基代替供试液,除不加菌外,其余操作同试验组,并进行微生物回收实验。阳性对照组。以等体积的胰酪大豆胨液体培养基代替供试液,其余操作同试验组。供试品对照组。不加菌外其他操作同试验组,见表2所列。
由表2可知,3批供试品组和阴性对照组都无菌生长,说明安中通便胶囊中对大肠埃希菌的检查可采用直接接种法。

2.2.4 微生物限度检查结果
3批安中通便胶囊中需氧菌总数<103 cfu/g、霉菌和酵母菌总数<102 cfu/g、大肠埃希菌均未检出,符合现行版药典关于中药制剂的微生物限度标准。
2.3 含量测定
2.3.1 色谱条件
Agilent的Zorbax Eclipse XDB型C18色谱柱(规格为250×4.6mm,5μm);甲醇-0.1%磷酸溶液(体积比85∶15)的流动相;流速设为1.0mL/min;柱温设为30 ℃;254nm 的检测波长;10μL的进样量。
2.3.2 供试品溶液的制备
取安中通便胶囊内容物3g,精密称定,置具塞锥瓶形中,精密加甲醇50mL,称重,回流1h,冷却,再次称重,甲醇补重,振摇均匀,滤过,精密量取10mL的续滤液,至烧瓶中,水浴锅上挥去甲醇溶剂后,再加入10mL盐酸溶液(体积分数为8%),振摇,再加入氯仿10mL,水浴锅上进行加热回流(1h),置分液漏斗中,静置20min,分取下层溶液,酸液再用氯仿进行提取(10mL/次,3次),然后合并氯仿萃取液,挥去溶剂,残渣加甲醇至5mL的量瓶中,过滤后取续滤液,即得。
2.3.3 大黄酚及大黄素对照品溶液的制备
称取大黄酚及大黄素对照品适量,精密称定,加入甲醇制成每1mL含大黄素40μg的溶液和每1mL含大黄酚60μg的混合溶液,即得。
2.3.4 安中通便胶囊阴性对照溶液的制备
按安中通便胶囊处方比例制备缺大黄的安中通便胶囊阴性样品。再按照2.3.2节方法制成缺大黄的安中通便胶囊阴性对照溶液。
2.3.5 安中通便胶囊方法学考察
分别吸取10μL的安中通便胶囊供试品溶液、大黄素、酚混合对照品溶液及缺大黄的安中通便胶囊阴性对照溶液,注入液相色谱仪中,按照上述色谱条件进行测定检测。安中通便胶囊供试品色谱峰中,大黄素:保留时间tR=7.698min,理论塔板数n=13 072;分离度R=3.72(R>1.5);拖尾因子T=0.96(0.95<T<1.05)。大黄酚:保留时间tR=9.526min,理论塔板数n=15 848;分离度R=5.47(R>1.5);拖尾因子T=1.04(0.95<T<1.05),均符合中国药典的规定。在上述的色谱条件下,大黄素和大黄酚均能与其他物质成分很好地分离,且保留时间与对照品一致;缺大黄的安中通便胶囊的阴性对照无干扰,其结果如图3所示。
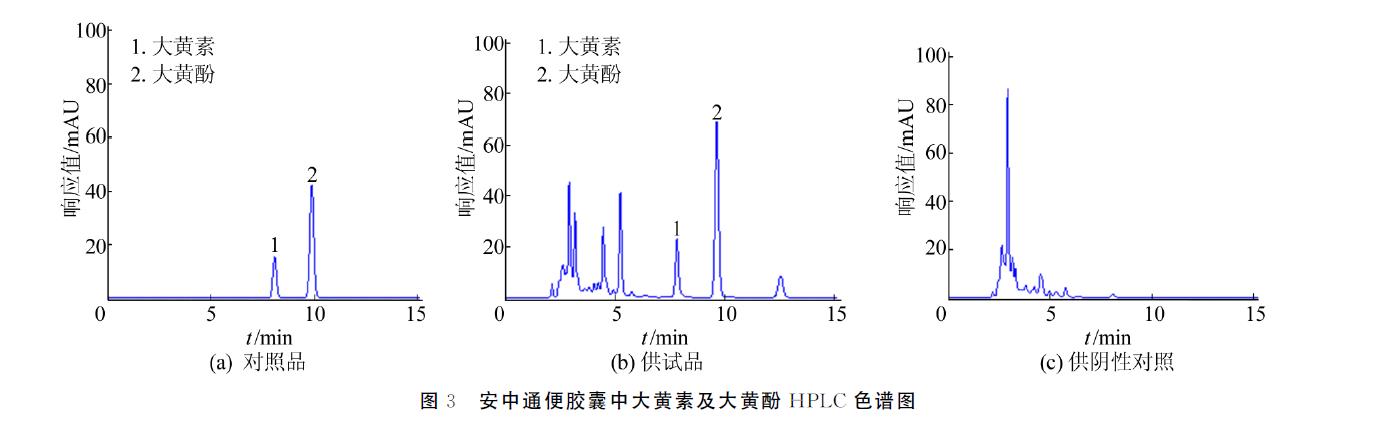
参照高效液相色谱法(现行版药典通则0512)进行试验,精密吸取混合对照品储备液0.25、0.50、1.00、2.00、4.00、6.00mL,分别置于容量瓶中(规格为10mL),用甲醇稀释至刻度,振
摇均匀。精密吸取不同质量浓度的大黄素和大黄酚对照品溶液各10μL注入液相色谱仪,按上述色谱条件测定,以大黄素及大黄酚的质量浓度(X)为横坐标,峰面积(A)为纵坐标,计算得到线性回归方程如下:
大黄素 A=33.267 33X+39.323 9 (r=0.999 7);大黄酚 A=48.145 94X+11.032 21(r=0.999 6)。结果表明:大黄素、大黄酚对照品的质量浓度
分别在0.006~0.144mg/mL、0.018~0.420mg/mL范围内,线性关系良好。精密吸取大黄素、酚混合对照品溶液10μL,注入至液相色谱仪中,连续进样6次,依法测定。结果显示,大黄素及大黄酚的精密度均良好,相对标准偏差(relative standard deviation,RSD)均为0.10%。精密吸取安中通便胶囊供试品溶液10μL,不同时间各进1次样,依法进行测定。结果表明,供试品中大黄素及大黄酚在10h内均稳定,RSD分别为0.72%和0.35%。精密称取安中通便胶囊样品3.0g(批号为20180310),平行6份,按2.3.2节方法制备安中通便胶囊的供试品溶液(编号1~6),依法进行测定。结果显示,大黄素及大黄酚两者的重复性均良好,RSD分别为1.57%和1.19%。称取同一批样品9份(大黄素0.646 8mg/g;大黄酚1.440 1mg/g)适量,分别精密加入大黄素及大黄酚混合对照品溶液适量,按2.3.2节方法制备安中通便胶囊供试品溶液,依法测定,大黄素及大黄酚的平均回收率分别为98.95%、96.77%,RSD分别为0.97%、0.84%。结果见表3、表4所列。
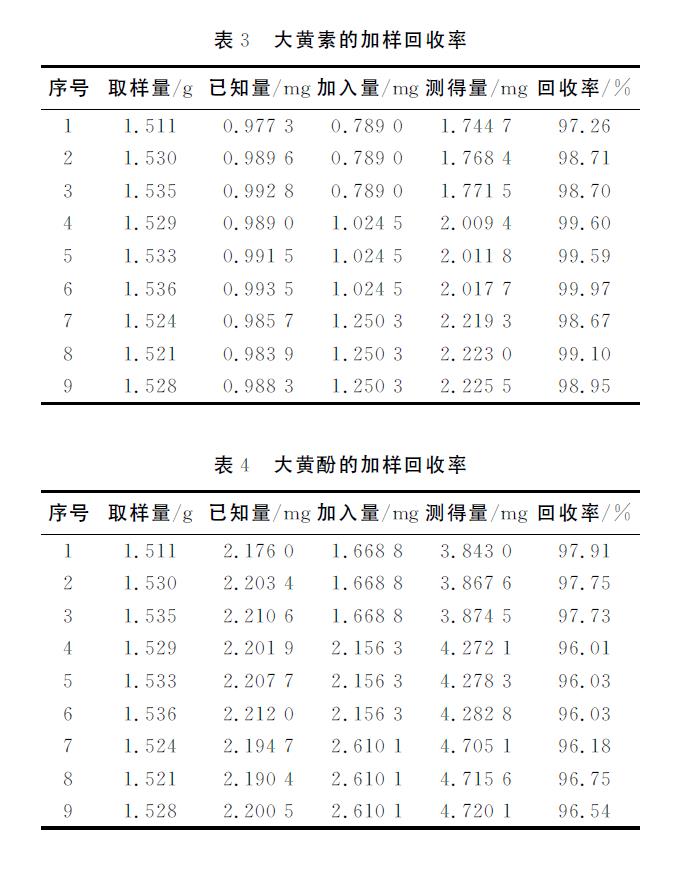
2.3.6 安中通便胶囊样品含量测定
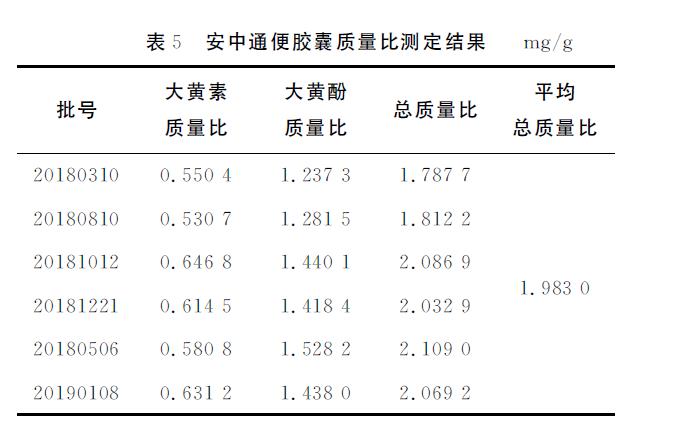
分别精密称取各批号(20180310、20180506、20180810、20181012、20181221、20190108)安中通便胶囊样品,按2.3.2节方法制备安中通便胶囊供试品溶液,进样测定,按外标法计算安中通便胶囊各批次样品质量比,结果见表5所列。
3 讨 论
3.1 定性鉴别
安中通便胶囊是安徽中医药大学第一附属医院的注册制剂品种,本课题组前期已采用薄层色谱法(TLC)对方中大黄、炒火麻仁和麸炒枳实进行相关定性鉴别[3],在此研究的基础上,对方中姜厚朴、肉苁蓉进行薄层鉴别研究,结果表明,以上2种药味的TLC鉴别方法专属性强,重复性好,阴性无干扰,建议纳入制剂质量标准。而方中炒白芍尚未建立合适的TLC鉴别方法。查阅文献发现,白芍所含的化学成分有芍药苷、牡丹酚、芍药花苷、挥发油、黄酮、多糖、鞣质、香草酸、β-谷甾醇和三萜类等成分,其中主要有效成分芍药苷、芍药内酯苷等单萜苷是白芍控制的指标性药效物质基础[8-9]。参照现行版《中国药典》,本文对炒白芍进行薄层定性鉴别研究,结果表明,供试品色谱中,在与对照药材相应的位置上未显示相同颜色的斑点,推测一方面是方中炒白芍所占处方比例较小,另一方面安中通便胶囊的制备工艺为水提工艺,未将其充分提取出来所致,因此仍需进一步
深入研究。
3.2 定量指标的选择
根据国家药品监督管理局《中药制剂质量及稳定性研究技术指导原则》的规定,以检测方中君臣药、贵重药和毒剧药为主的原则。方中大黄泻下攻积、清热泻火、凉血解毒、逐瘀通经为君药,麸炒枳实、炒瓜蒌子、姜厚朴、肉苁蓉润肠通便,益精710 合肥工业大学学报(自然科学版) 第43卷 血以助君药之功为臣药。现行版《中国药典》一部收载了HPLC法测定大黄中芦荟大黄素(C15H10O5)、大黄酸(C15H86)、大黄素(C15H10O5)、大黄酚(C10H10O4)和大黄素甲醚(C16H12O5)总量的方法。因此,可采用游离的大黄蒽醌类化合物为定量指标作为该制剂的质量控制指标。同时,通过文献[10]及预实验发现,安中通便胶囊中大黄素和大黄酚的色谱峰分离良好,峰形对称,为主要色谱峰,故选取大黄素和大黄酚作为测定指标,并建立了本品中大黄素和大黄酚的高效液相色谱测定法。经方法学考察,本方法简便、准确、可靠、重现性好,可作为本品质量控制的定量指标。
3.3 活性成分的作用机理探讨
安中通便胶囊在临床使用近20年,对慢传输型等便秘疗效尤其显著,可改善便秘症状,其作用机制可能与其提高结肠组织Cajal间质细胞(interstitial cells of Cajal,ICC)表达量,降低神经递质一氧化氮(nitric oxide,NO)、一氧化氮合酶(nitric oxide synthase,NOS)的水平,提高结肠组织ICC 的表达量及修复SCF/c-kit 信号通路有关[11-12]。根据目前的大量文献报道,方中的大黄蒽醌类成分及其代谢产物主要作用于结肠,可通过刺激肠黏膜及肌肠间神经,增加肠推动性蠕动,促进水和电解质的分泌使粪便变得稀、软,利于排便[13]。另外,相关代谢产物还能引起5-HT、组胺增加,抑制Na+ -K+ -ATP酶活性,潴留水分在肠腔,增加肠道容积,起容积性泻药的作用[14]。基于以上,本文认为安中通便胶囊中的大黄蒽醌类对便秘的治疗起到重要作用,具体作用机制有待进一步探讨和深入研究。
4 结 论
本文提出的薄层鉴别方法能准确鉴别安中通便胶囊中姜厚朴、肉苁蓉2种药味;提出的HPLC含量测定方法可准确对制剂中2种有效成分进行控制,并按现行版药典方法进行了微生物限度检查验证,方法可行,适用于安中通便胶囊微生物限度检查。所拟定的新质量标准草案可更准确地控制安中通便胶囊药品质量。
[参 考 文 献]
[1] 李明,王建民.安中通便胶囊治疗慢性功能性便秘40例临床观察[C]//2007年全国便秘的基础研究与临床诊治新概念学术会议论文集.厦门:中华医学会中华胃肠外科杂志编辑部,2007:102-103.
[2] 李林,王翼洲,朱春冬,等.安中通便胶囊合西药治疗老年功能性便秘50例[J].安徽中医学院学报,2008,27(4):8-9.
[3] 孟楣,黄非.安中通便胶囊的定性定量研究[J].中国中医药信息杂志,2006,13(1):42-43.
[4] 徐乐,孔亚萍,孙慧珠.舒肝丸质量标准中薄层和液相方法完善研究[J].中国药事,2018,32(4):516-521.
[5] 国家药典委员会.中华人民共和国药典(2015年版一部)
[M].北京:中国医药科技出版社,2015:251-135.
[6] 王秀琴,王东兴,纪丽颖,等.薄层色谱法鉴别参萸清眩膏
[J].华南国防医学杂志,2017,31(9):631-634.
[7] 国家药典委员会.中华人民共和国药典(2015年版四部)
[M].北京:中国医药科技出版社,2015:140-374.
[8] 章丽,赵冰洁,袁嘉瑞,等.基于“组分结构”理论对丹皮、赤芍和白芍化学成分的对比研究[J].中国中药杂志,2016,41(10):1835-1842.
[9] 任娟,刘晓,李伟东,等.基于UHPLC-Q-TOF-MS/MS 的白芍炒制前后化学成分研究[J].世界中医药,2019,142(2):268-273.
[10] 陈学艳,张敏娟,魏文芝,等.8种复方龙胆碳酸氢钠片中5种蒽醌苷含量比较研究[J].西南国防医药,2019,29(11):1096-1099.
[11] 王建民,李明,唐冉,等.益气健脾通便方对慢传型便秘大鼠结肠组织ICC及SCF/c-kit信号通路的影响[J].中华中医药学刊,2019,37(1):154-158.
[12] 王建民,王培森,唐冉.益气健脾通便方对慢传输型便秘大鼠Cajal间质细胞及一氧化氮、一氧化氮合酶的影响[J].安徽中医药大学学报,2018,37(1):58-62.
[13] 李景,金鹏,刘喜纲.大黄蒽醌类成分在胃液中的稳定性及其肠溶化增效作用分析[J].中国实验方剂学杂志,2018,24(10):21-26.
[14] 计树灵,韩佳瑞,贺璐璐,等.大黄素对洛哌丁胺致小鼠便秘的治疗作用[J].中国病理生理杂志,2019,35(12):2262-2268.
公司:win德赢官方
地址:新疆和田洛浦县杭桂路232号
公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
