


















公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
公司地址:新疆和田洛浦县杭桂路232号
杨瑞瑞1 乔蓉霞1
杜宏伟2 李卓敏2
( 1. 陕西省食品药品检验所,西安,710061;2. 西安正大制药有限公司,西安,710043)
摘要:目的 完善补脑丸质量标准。 方法 采用薄层色谱鉴别补脑丸中的当归、枸杞子、肉苁蓉、酸枣仁,采用RP- ELSD-HPLC 测定酸枣仁中酸枣仁皂苷A 的含量。结果 在薄层色谱中分别检出当归、枸杞子、肉苁蓉、酸枣仁,斑点清晰,重现性好。RP- ELSD-HPLC 得到酸枣仁皂苷A 的线性范围在0.498μg~24.9μg 之间,γ=0.999;平均回收率为95.47%,RSD 为6.35%(n=6)。结论 定性定量方法简便、专属、准确,提高了补脑丸药品的控制标准。
关键词:薄层色谱法;酸枣仁皂苷A;高效液相色谱法
补脑丸[1]收载于《卫生部药品标准中药成方制剂第十册》,是由酸枣仁、当归、 枸杞子、 肉苁蓉、五味子等多味中药组成的复方制剂,具有滋补精血,健脑益智,安神镇惊,化痰熄风。临床上用于治疗迷惑健忘,记忆减退,头晕耳鸣,心烦失眠,心悸不宁,癫痫头痛,神烦胸闷等。原质量标准中只有当归、五味子等几味药的显微特征鉴别,为了更好的控制该制剂的内在质量,对本品分别用薄层色谱法和高效液相色谱法进行了定性定量研究。
1 仪器、试剂与试药
Waters -Alliance 2695-2487(YY01520041103)高效液相色谱仪,蒸发光散射检测器 (Alltech ELSD 2000),色谱柱:kromasil C18 柱(5μm,250×4.6mm);乙腈为色谱纯,水为高纯水,其它试剂均为分析纯。酸枣仁皂苷A 对照品(批号为110734-200509)、酸枣仁皂苷B 对照品(批号为1110814-200506)、枸杞子对照药材(批号121072-0301)、松果菊苷对照品(批号为111670-200401,中检所提供)、当归对照药材 (批号120927-200310)均由中国药品生物制品检定所提供。补脑丸样品及实验用阴性样品均由西安正大制药有限公司提供。
2 定性鉴别
2.1 当归的鉴别
2.1.1 对照药材溶液的制备 取当归对照药材1g,加乙醚20m1,超声处理10分钟,滤过,滤液挥干,残渣加乙醇2ml 使溶解,作为对照药材溶液。
2.1.2 供试品溶液的制备 取本品适量,除去包衣,研细,取1g,加乙醚20m1,超声处理10 分钟,滤过,滤液挥干,残渣加乙醇2ml 使溶解,作为供试品溶液。
2.1.3 阴性样品溶液的制备 取不含当归的阴性样品1g,按“2.1.2”项下方法进行制备,作为阴性样品溶液。
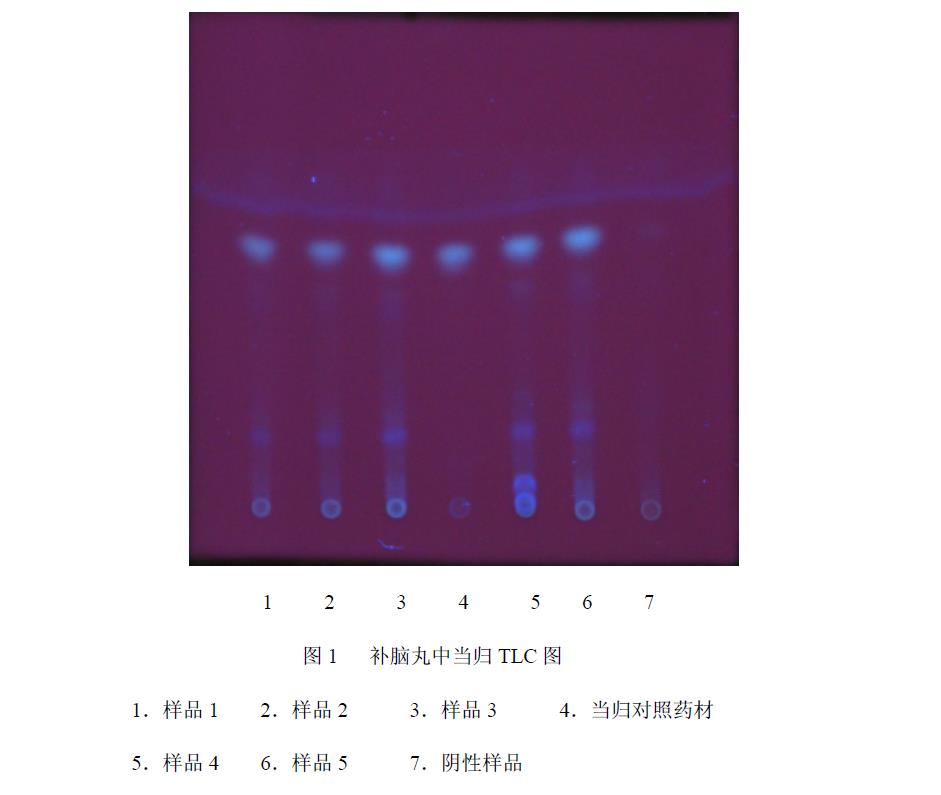
2.1.4 薄层色谱鉴别 吸取对照药材溶液、供试品溶液、阴性样品溶液各5μl,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G 薄层板上,以正己烷-乙酸乙酯(4∶1)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性样品无干扰。见图1。
2.2 肉苁蓉的鉴别
2.2.1 对照品溶液的制备 取松果菊苷对照品,加甲醇制成每1ml 含0.5mg 的溶液,作为对照品溶液。
2.2.2 供试品溶液的制备 取本品适量,除去包衣,研细,取1g,加甲醇20ml,超声处理15 分钟,滤过,滤液浓缩至近干,残渣加甲醇2ml 使溶解,作为供试品溶液。
2.2.3 阴性样品溶液的制备 取不含肉苁蓉的阴性样品1g,按“2.2.2”项下方法进行制备,作为阴性样品溶液。
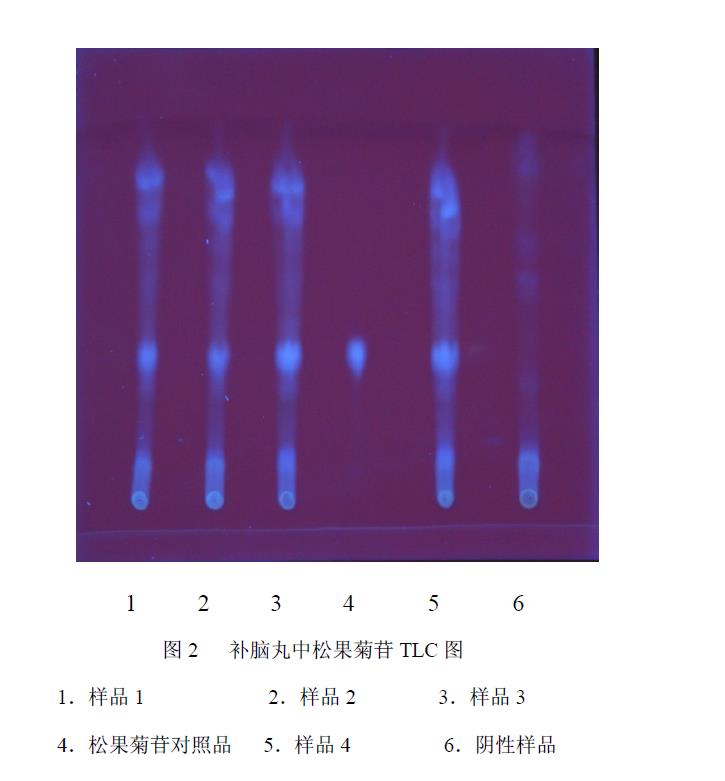
2.2.4 薄层色谱鉴别 吸取对照品溶液、供试品溶液、阴性样品溶液各1μl ,分别点于同一聚酰胺薄膜上,以甲醇-醋酸-水(2∶1∶7)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性样品无干扰。见图2。
2.3 枸杞子的鉴别
2.3.1 对照药材溶液的制备 另取枸杞子对照药材0.5g,加水50ml,加热煮沸15 分钟,放冷,滤过,滤液用乙酸乙酯25ml 振摇提取,提取液浓缩至约1ml,作为对照药材溶液
2.3.2 供试品溶液的制备 取本品适量,除去包衣,研细,取5g,加水50ml,加热煮沸15 分钟,放冷,滤过,滤液用乙酸乙酯25ml 振摇提取,提取液浓缩至约1ml,作为供试品溶液。
2.3.3 阴性样品溶液的制备 取不含枸杞子的阴性样品5g,按“2.3.2”项下方法进行制备,作为阴性样品溶液。
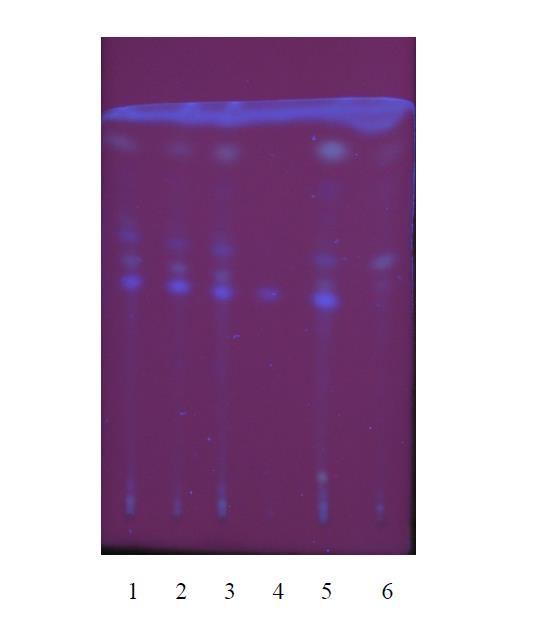
2.3.4 薄层色谱鉴别 吸取对药材溶液、供试品溶液、阴性样品溶液各5μl,分别点于同一以羧甲基纤维素钠为粘合剂的硅胶G 薄层板上,以甲苯-乙酸乙酯-甲酸(10∶5∶2)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。阴性样品无干扰。见图3。
2.4 酸枣仁的鉴别
2.4.1 对照品溶液的制备 取酸枣仁皂苷A 和酸枣仁皂苷B 对照品适量,加甲醇分别制成每1ml 含0.5mg 的溶液,作为对照品溶液。
2.4.2 供试品溶液的制备 取【含量测定】项下的供试品溶液作为供试品溶液。
2.4.3 阴性样品溶液的制备 取不含酸枣仁的阴性样品5g,按“2.4.2”项下方法进行制备,作为阴性样品溶液。
2.4.4 薄层色谱鉴别 吸取酸枣仁皂苷A 对照品溶液与酸枣仁皂苷B 对照品溶液各5μl,供试品溶液、阴性样品溶液各10μl,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶 G薄层板上,以正丁醇-冰醋酸-水(4∶1∶5)的上层溶液为展开剂,展开,取出,晾干。喷以2%香草醛硫酸溶液,在100℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。阴性样品无干扰。见图3。

3 RP-HPLC 测定补脑丸中酸枣仁皂苷含量
3.1 色谱条件
色谱柱: Kromasil 色谱柱(C18,5μm,250×4.6mm);柱温:30℃; 流动相: 乙腈—水 (33:67) ;流速: 1.0ml/min ;气流:2.5 ml/min ;漂移管温度:110℃。
3.2 对照品溶液的制备 精密称取酸枣仁皂苷A 对照品适量,加甲醇制成每1ml含0.2mg 的溶液。
3.3 供试品溶液的制备 取本品适量,除去包衣,研细,精密称取5g,置于索氏提取器中,加乙醚适量回流提取3 小时,醚液弃去。药渣挥尽残醚,再加甲醇适量回流提取5 小时。甲醇提取液置水浴上蒸干,残渣加水20ml,分数次定量转移到分液漏斗中。用水饱和的正丁醇提取5 次,每次15ml。合并正丁醇提取液,用正丁醇饱和的氨水(取40ml 浓氨溶液加水稀释到100ml,再用正丁醇饱和。分取下层液)洗涤2 次,每次50ml,洗液弃去,再用正丁醇饱和的水洗涤2次,每次50ml,正丁醇提取液置水浴上蒸干。残渣加甲醇溶解,定量转移至5ml容量瓶中,加甲醇稀释至刻度,摇匀,作为供试品溶液。
3.4 阴性样品溶液的制备 取不含酸枣仁的阴性样品,按“3.3”项下的制备方法,同法制成阴性样品溶液。
3.5 方法学考察
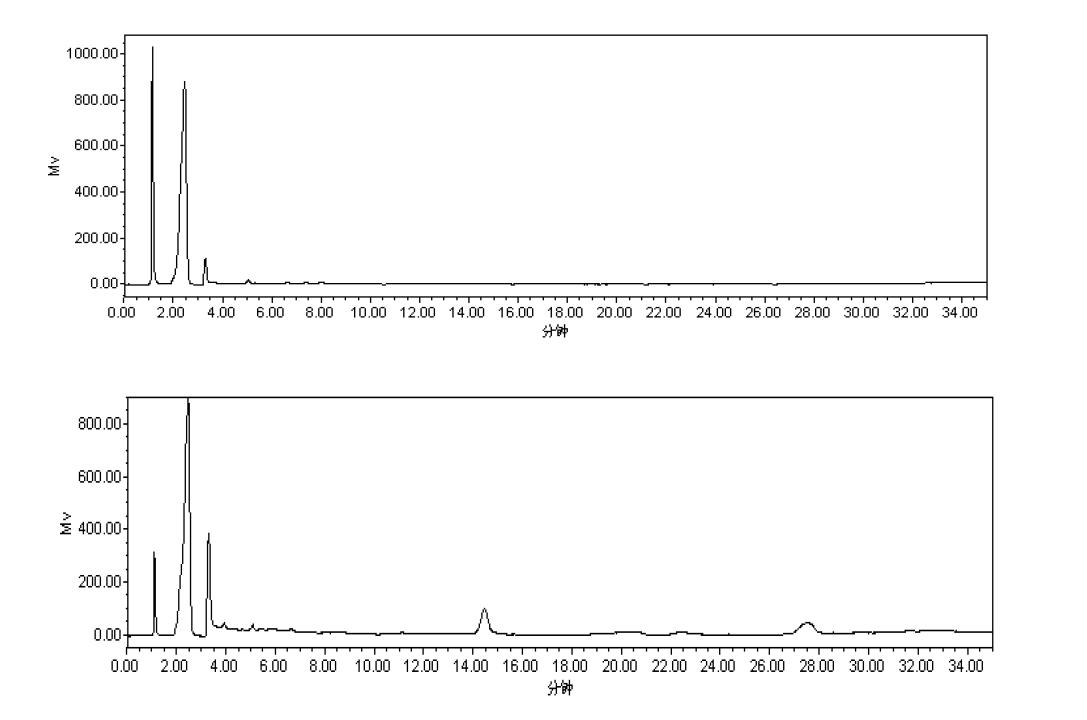
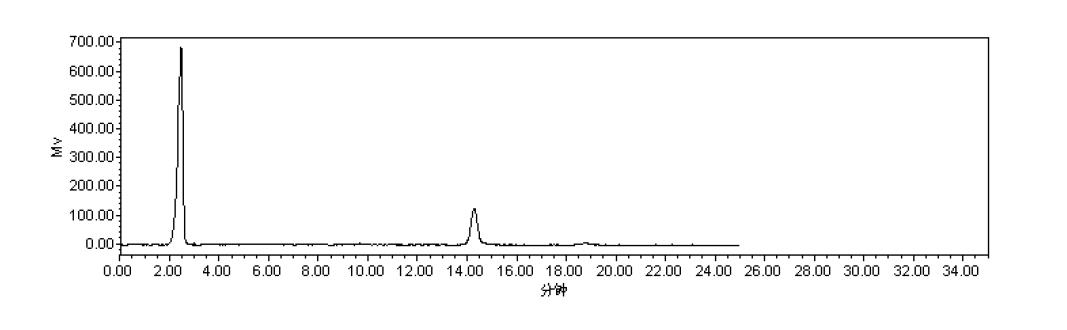
3.5.1 线性范围考察 精密称取酸枣仁皂苷A 对照品12.45mg,置25ml 量瓶中,加甲醇溶解并稀释至刻度,摇匀,即浓度为0.498mg/ml,按上述色谱条件,分别进样1μl、2μl、5μl、10μl、15μl、20μl、25μl、30μl、40μl、50μl,记录色谱图,计算峰面积,以峰面积的对数值与进样量的对数值进行回归,求得回归方程为:Y=1.4102X+5.7014,R=0.999,表明酸枣仁皂苷A 在0.498μg~24.9μg 之间线性良好。
3.5.2 精密度考察 取按“3.3”制备的样品溶液,重复进样6 次,按“3.1”项下色谱条件进行测定,记录峰面积,计算相对标准偏差为4.01%。表明仪器精密度良好。
3.5.3 稳定性考察 取按“3.3”制备的样品溶液,24 小时内分别进样5 次,记录峰面积,计算相对标准偏差为4.80%。表明样品溶液在24 小时内基本稳定。
3.5.4 重复性考察 精密取同一批次样品6 份,分别按“3.3”项下的供试品溶液制备方法制备供试品溶液,按“3.1”项下色谱条件进行测定,计算其相对标准偏差为5.33%。
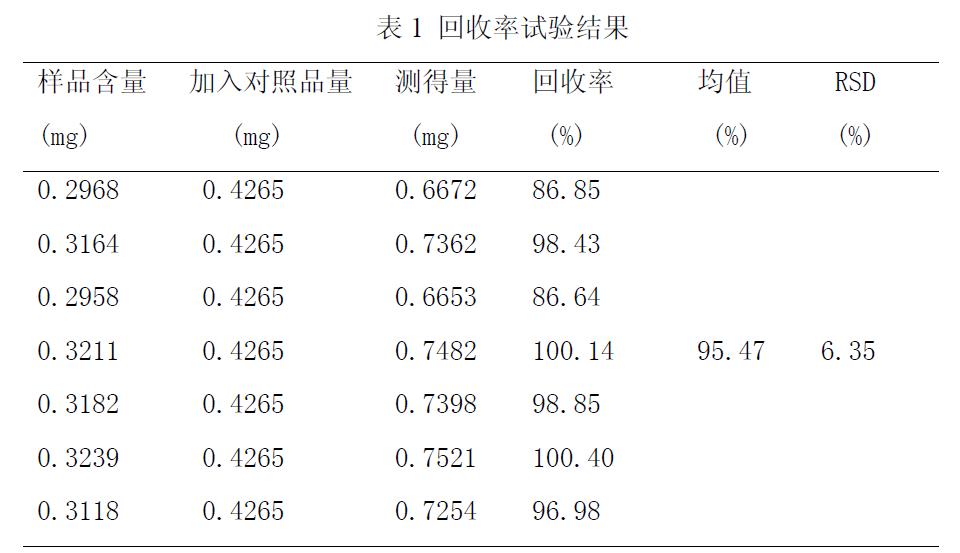
3.5.5 加样回收率试验 精密称取重复性试验样品细粉共6 份,每份2.5g,分别精密加入酸枣仁皂苷A 对照品溶液(0.4265mg/ml)1ml,挥干,按“3.3”项下的供试品溶液制备方法制备供试品溶液,按“3.1”项下色谱条件进行测定,结果见表1
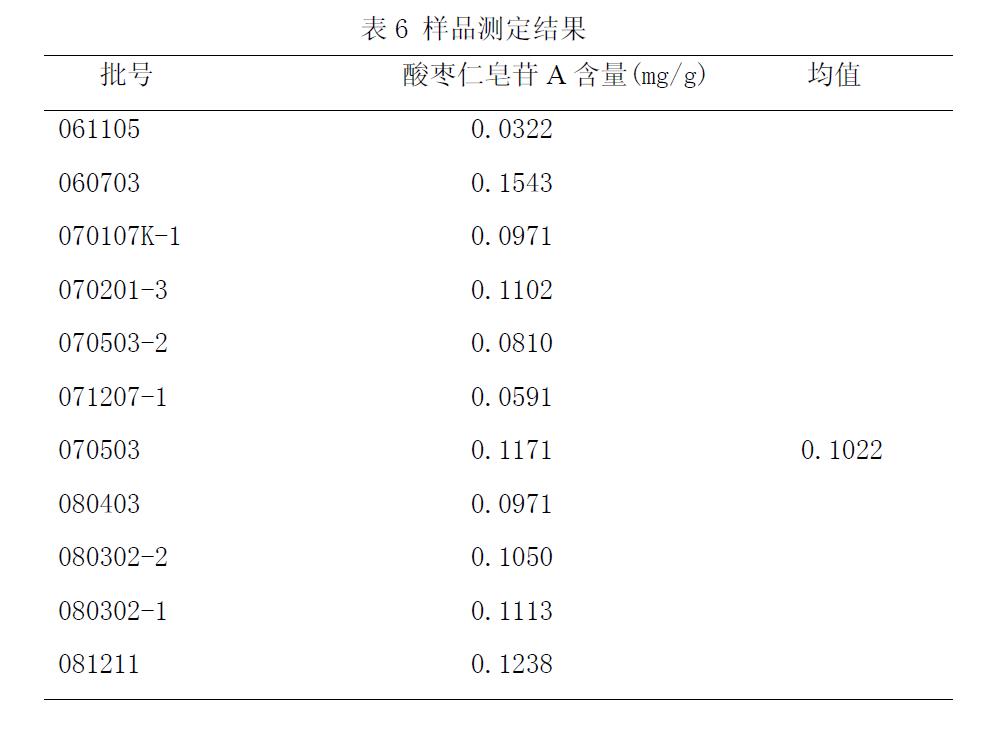
3.6 样品含量测定
收集到的13 批样品,分别按按“3.3”项下的供试品溶液制备方法制备供试品溶液,按“3.1”项下色谱条件进行测定,结果见表2。
4 讨论
4.1 补脑丸中的酸枣仁[2]具有养心安神的功效,其中所含的酸枣仁皂苷A 及B为有效成分之一。酸枣仁皂苷A 及B 的含量测定方法以前多采用薄层扫描法[3],近来有采用高效液相色谱法测定。本实验在查阅有关资料[4][5]后,对补脑丸主要药味酸枣仁中的酸枣仁皂苷A 用高效液相色谱法进行了测定,结果表明,该方法简便、准确、重现性好,可有效地控制其质量。
4.2 在预试验中,对样品供试品溶液制备中的取样量、提取溶剂、提取时间、除杂溶剂及用量等进行了多因素考察,以乙醚脱脂、甲醇提取、正丁醇萃取、氨溶液除杂质为较优条件。对于色谱条件也进行了优化,比较了甲醇-水系统和乙腈-水系统,以乙腈-水(33∶67)为优;由于用的是空气源,所以气流速为2.5ml/min,漂移管温度为110℃。
4.3 薄层色谱鉴别中当归、枸杞子用对照药材作对照,均能得到满意的层析结果;肉苁蓉因有二种,薄层色谱不完全一致,选用松果菊苷和毛蕊花糖苷作对照,样品中在与毛蕊花糖苷斑点相同位置有干扰,故只选松果菊苷作对照;酸枣仁皂苷B 在含量测定中量较小,未作为控制指标,增加在薄层色谱鉴别中。
参考文献:
[1]《卫生部药品标准中药成方制剂第十册》
[2]《中国药典2005 年版一部》
[3]尹清茹,张永玲.薄层扫描法测定咽炎丸中酸枣仁皂苷的含量. 中国药业,1999,8(8):34~35
[4]钟东会,雷根虎,郭五保等. RP-HPL 测定酸枣仁中的酸枣仁皂苷A 的含量. 中成药,2004, 26 (11):963~964
[5]李会军,李萍. 高效液相色谱法蒸发光散射检测器测定酸枣仁皂苷A 及B 的含量. 药物分析杂志,2000,20(2):82~84
公司:win德赢官方
地址:新疆和田洛浦县杭桂路232号
公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
