


















公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
公司地址:新疆和田洛浦县杭桂路232号
帖晓燕1,冯银平1,马冬妮1,张云鹤1,张文广1,王丹1,樊秦2,李芸1
(1.甘肃中医药大学,甘肃兰州730000;2.甘肃省中藏药化学与质量研究省级重点实验室,甘肃兰州730000)
摘要:探讨产地蒸制加工对荒漠肉苁蓉药材质量的影响,为肉苁蓉的产地加工提供科学依据。新鲜的荒漠肉苁蓉刷去表面浮土,刮去表皮鳞叶,后根据其粗细、长短规格进行大小分档并蒸制(蒸至透心为止),将直径
为3.0~4.0 cm、4.0~4.5 cm、4.5~5.0 cm 的肉苁蓉分别蒸制10 min、12~13 min、15~16 min,然后在70 ℃下烘至七八成干,切成不同规格的饮片和丁,按照《中华人民共和国药典》(2015 年版)方法分别测定水溶性浸出物,醇溶性浸出物,松果菊苷和毛蕊花糖苷的含量。结果表明,肉苁蓉的浸出物均符合《中华人民共和国药典》规定,且以5~10 mm 饮片为佳,新鲜肉苁蓉药材的松果菊苷和毛蕊花糖苷的含量明显不达标,但经过产地加工,肉苁蓉的含量均都达到《中华人民共和国药典》要求,且1.5 cm 丁的质量较好,经过蒸制加工后的肉苁蓉较新鲜药材质量明显提高。产地蒸制加工对肉苁蓉的质量影响显著,为肉苁蓉合理的产地加工提供科学依据。
关键词:肉苁蓉;蒸制加工;浸出物;松果菊苷;毛蕊花糖苷
肉苁蓉为列当科植物肉苁蓉Cistanche deserticola Y.C. Ma 和德赢vwin登录 Cistanche tubulosa(Schenk)Wight 的干燥带鳞叶的肉质茎[1],主产于内蒙古、新疆、甘肃等地,主要生长在盐碱地、戈壁沙漠一带,主要寄生在红柳、莎莎、西伯利亚白刺等植物的根上。《神农本草经》将肉苁蓉归为上品,又有肉松容、黑司命之称[2]。有研究表明,肉苁蓉总寡糖、去半乳糖醇总寡糖和半乳糖醇是肉苁蓉通便的主要活性成分[3]。肉苁蓉中含有苯乙醇苷类、生物碱、多糖[4]等多种成分。其中,苯乙醇苷类具有重要的神经保护作用,常用于治疗和预防帕金森病[5-6]。产地加工是中药材生产的第一个环节,也是最关键的一步。《中华人民共和国药典》记载肉苁蓉的产地加工为:除去茎尖,切段,晒干[1]。荒漠肉苁蓉的传统产地加工方法为在出土前被挖去带有鳞片的肉质茎,干燥后即可作为药用[7]。现代常常采用蒸制加工处理的方法,以此来尽可能保留或提高肉苁蓉中的醇溶性成分及苯乙醇苷类等有效成分的含量[8]。但荒漠肉苁蓉的肉质茎比较粗壮,采收期天气比较寒冷,太阳光较少,很不容易干燥,药材极易发生霉烂变质,而且好不容易干燥的药材,在炮制成饮片时需进行二次闷润,难免会造成水溶性成分的流失,从而影响了药材的品质和临床疗效。而趁鲜蒸制加工并切制干燥,将采挖的新鲜肉苁蓉直接蒸制加工,再切制干燥,即在产地就形成中药饮片,减少中间形成干药材的环节,既能避免有效成分的损失,又能降低成本。笔者等以探讨产地蒸制加工对荒漠肉苁蓉质量的影响为目的,为规范肉苁蓉的产地加工提供科学依据。
1 仪器与试药
1.1 仪器
Agilent 1260Ⅱ型高效液相色谱仪(美国Agilent 科技有限公司,DAD 检测器);MA37 型快速水分测定仪(赛多利斯科学仪器有限公司);BT125D 型1/10 万电子天平(赛多利斯科学仪器有限公司);KQ3200DB 型超声波清洗器(昆山市超声仪器有限公司);FW-400A 型高建万能粉碎机(北京科伟永兴仪器有限公司);SHB-3 型循环水多用真空泵(郑州杜甫仪器厂);DHG-9240A 型电热恒温鼓风干燥箱(上海一恒科技有限公司)。
1.2 试剂
松果菊苷对照品(批号CHB170302,HPLC ≥98%)、毛蕊花糖苷对照品(批号CHB171103,纯度≥98%)均购自成都克洛玛生物科技有限公司;甲醇均为色谱纯;45%乙醇为分析纯;水为娃哈哈纯净水。
1.3 药材
实验用荒漠肉苁蓉采挖自内蒙古阿拉善盟左旗,经甘肃中医药大学附属医院杨锡仓主任中药师鉴定为列当科植物肉苁蓉Cistanche deserticola Y. C. Ma 的干燥带鳞叶的肉质茎。新鲜采挖的肉苁蓉水分为71.22%。
2 方法与结果
2.1 新鲜肉苁蓉的加工处理
新鲜荒漠肉苁蓉刷去表面浮土,刮去表皮鳞叶,后根据其粗细长短规格进行大小分档并蒸制(蒸至透心为止),将直径为3~4 cm 的蒸制10 min;直径为4.0~4.5 cm 的肉苁蓉蒸制12~13 min;直径为4.5~5 cm 肉苁蓉蒸制15~16 min,然后在70 ℃下烘至水分约20%时(七八成干),切成不同规格的片和丁。见表1。

2.2 水分测定
取样品粉末(过3 号筛)约3.0 g,精密称定,使用快速水分测定仪测定,每个样品平行测定3 次。结果见表2。2.3 浸出物测定[9]
2.3.1 水溶性浸出物取样品粉末(过4 号筛)约3.0 g,精密称定,照《中华人民共和国药典》2015 年版四部(通则2201),采用水为溶剂以冷浸法进行测定,每个样品平行3份。结果见表2。
2.3.2 醇溶性浸出物取样品粉末(过4 号筛)约3.0 g,精密称定,照《中华人民共和国药典》2015 年版四部(通则2201),采用稀乙醇为溶剂以冷浸法进行测定,每个样品平行3 份。结果见表2。
2.4 松果菊苷和毛蕊花糖苷含量测定[1]
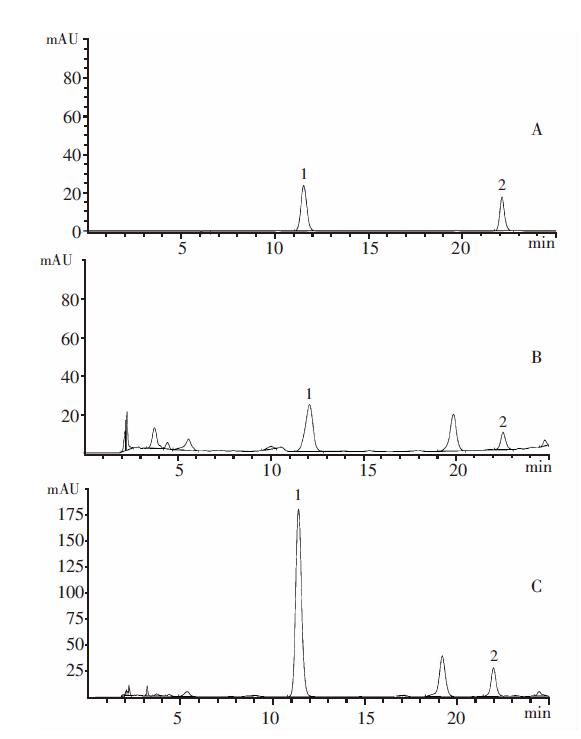
2.4.1 色谱条件参考《中华人民共和国药典》2015 年版(一部)肉苁蓉项下含量测定方法优化。色谱柱为AgilentExtend C18(4.6 mm×250 mm,5 μm),以甲醇为流动相A,0.1%甲酸溶液为流动相B 进行梯度洗脱(0~15 min,26.5% A;15~20 min,26.5%~35%A;20~25 min,35%~40% A),流速为1.0 mL/min,柱温为30 ℃,进样量为10 μL,检测波长为330 nm。色谱图见图1。
2.4.2 混合对照品溶液的制备取松果菊苷对照品、毛蕊花糖苷对照品适量,精密称定,加50%甲醇制成每1 mL分别含1 mg 松果菊苷和0.495 mg 毛蕊花糖苷的混合溶液,即得。
2.4.3 供试品溶液的制备取本品粉末(过4 号筛)约1 g,精密称定,置100 mL 棕色量瓶中,精密加入50%甲醇25 mL,密塞,摇匀,称定重量,浸泡30 min,超声处理40 min
(功率250 W,频率35 kHz),放冷,再称定质量,用50%甲醇补足减失的质量,摇匀,静置,取上清液,滤过,取续滤液,即得。
2.4.4 方法学考察
2.4.4.1 线性关系考察精密吸取混合对照品溶液0.02 mL、0.04 mL、0.10 mL、0.20 mL、0.40 mL、1.00 mL,分别置5.00 mL 量瓶中,加入50%甲醇定容,摇匀,按上述色谱条件注入色谱仪,记录峰面积,以质量浓度为横坐标(X),峰面积值为纵坐标(Y),绘制标准曲线。
2.4.4.2 精密度试验取混合对照品溶液,按上述色谱条件重复进样6 次,依法测定。
2.4.4.3 重复性试验取S1 样品,按上述供试品溶液的制备方法平行制备6 份,依法测定。
2.4.4.4 稳定性考察取S1 样品溶液,分别于配制后0 h、2 h、4 h、6 h、10 h、24 h 进样,依法测定。
2.4.4.5 样品含量测定分别精密称取S0~S6 样品,按上述供试品溶液的制备方法分别制样,依法测定,计算党参炔苷的含量。结果见表2。
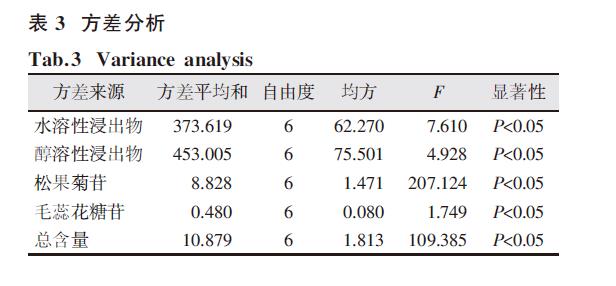
2.5 产地加工不同规格肉苁蓉水分测定结果结果见表2。由表2 可知,产地加工不同规格肉苁蓉(无论是片或丁)蒸制加工后的饮片水分均比新鲜药材低。经过蒸制加工,肉苁蓉不同规格的饮片水分均比新鲜时的低,且3 种规格下饮片的水分均比3 种规格的丁低。
2.6 产地加工不同规格肉苁蓉浸出物测定结果由表2 可知,产地加工不同规格的肉苁蓉经过蒸制加工后,无论是片还是丁,其水溶性浸出物均高于新鲜药材;3 种规格下片的醇溶性浸出物均高于新鲜药材,但3 种规格下丁的醇溶性浸出物却低于新鲜药材。且水溶性浸出物和醇溶性浸出物最高的均为0.5~1.0 cm 的片。
2.7 方法学考察结果
松果菊苷回归方程为Y=7 346X-23.749,r=0.999 9,毛蕊花糖苷回归方程为Y= 8 783.8X-10.522,r=0.999 9。结果表明松果菊苷在0.004~1.000 mg/mL 范围内线性关系良好;松果菊苷和毛蕊花糖苷峰面积的RSD 分别为
0.18%和0.14%,表明仪器的精密度良好;松果菊苷和毛蕊花糖苷含量RSD 分别为5.54%和3.65%,表明该方法重复性良好;松果菊苷和毛蕊花糖苷峰面积的RSD 分别为0.16%和0.47%,表明样品中松果菊苷和毛蕊花糖苷在24 h内稳定性良好;新鲜的荒漠肉苁蓉松果菊苷和毛蕊花糖苷的总含量仅为0.13%,不符合《中华人民共和国药典》标准(不低于0.3%),但经过蒸制切制成不同规格的饮片后,其总含量均达到《中华人民共和国药典》要求,其总含量由高到低依次为1.5 cm 丁>(0.5~1.0)cm 片>2.0 cm 丁>0.5 cm片>1.0 cm 丁>1.0 cm 片。
2.8 统计分析
结果见表3。由方差分析结果可得,与新鲜的荒漠肉苁蓉相比,肉苁蓉不同规格干燥品的水溶性浸出物、醇溶性浸出物、松果菊苷、毛蕊花糖苷、总含量指标均具有显著的统计学差异。
3 讨论
3.1 肉苁蓉的产地加工主要以蒸制为主,研究表明,蒸制可显著提高肉苁蓉中苯乙醇苷类成分的含量[10-11]。课题组对蒸制前后的肉苁蓉进行比较,发现蒸制后,肉苁蓉质变软,颜色变深,并伴有烤红薯气味,蒸制后肉苁蓉的品质较新鲜肉苁蓉有了很大提高,关于是否与蒸制后使其颜色变化,产生气味的物质基础有关,还有待进一步研究与探讨。
3.2 趁鲜蒸制加工并切制干燥,避免了传统炮制过程中因“二次闷润”造成有效成分的损失,从而提高药材品质和临床疗效。目前,常常会将肉苁蓉切制成约5 mm 的厚片[10,12-13],而未见有相关研究关于其他规格下的肉苁蓉质量检测情况。笔者对蒸制后的肉苁蓉进行了不同规格的切制,分别为5 mm、5~10 mm、10 mm 的厚片和10 mm、15 mm、20 mm 的丁,研究结果表明,15 mm 丁和5~10 mm 厚片相较于其他规格质量最佳,可在实际生产中切制成此类规格,即能保证质量,又便于临床调剂。
3.3 本研究以探讨鲜药材在经过产地加工过程化学成分的变化为目的,以水溶性浸出物、醇溶性浸出物、松果菊苷、毛蕊花糖苷的含量为考察指标,科学合理,为肉苁蓉产地加工规范化生产提供参考,也为以肉苁蓉为核心研发系列产品提供依据。
参考文献:
[1] 国家药典委员会. 中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015:135-136.
[2] 沈连生.神农本草经中药彩色图谱[M].北京:中国中医药出版社,1996:93-94.
[3] 高云佳,姜勇,戴昉,等.肉苁蓉润肠通便的药效物质研究[J].中国现代中药,2015,17(4):307-310+314.
[4] 龚千锋.中药炮制学[M].9 版.北京:中国中医药出版社,2015:347.
[5] SHENG G,PU X,LEI L,et al.Tubuloside B from Cistanchesalsa rescues the PC12 neuronal cells from 1-methyl-4-phenylpyridinium ion -induced apoptosis and oxidativestress[J].Planta Medica,2002,68(11):966-970.
[6] GENG X,SONG L,PU X,et al.Neuroprotective effectsof phenylethanoid glycosides from Cistanches salsa against1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine(MPTP)-induced dopaminergic toxicity in C57 mice [J].Biological& Pharmaceutical Bulletin,2004,27(6):797.
[7] 刘文静,曹妍,宋青青,等.荒漠肉苁蓉花及木质化茎的化学成分定性分析[J].中国中药杂志,2018,43(18):3708-3714.
[8] 彭芳,徐荣,高晓霞,等.蒸制和切片对产地加工肉苁蓉药材主要化学成分含量影响[J].现代中药研究与实践,2016,30(4):8-11.
[9] 国家药典委员会.中华人民共和国药典:四部[S]. 北京:中国医药科技出版社,2015:2101.
[10] 范亚楠,黄玉秋,贾天柱,等.星点设计-效应面法优化肉苁蓉软化切制工艺[J].中药材,2017,40(3):656-659.
[11] 彭芳,徐荣,王夏,等.不同等级整株肉苁蓉的药材品质和产地加工蒸制时间研究[J].中药材,2016,39(2):302-306.
[12] 姜勇,鲍忠,孙永强,等.肉苁蓉片的炮制工艺研究[J].中国药学杂志,2011,46(14):1074-1076.
[13] 梁淑燕,卢丹逸,耿宗成,等.提高肉苁蓉中苯乙醇苷类成分含量的加工方法研究[J].中国现代中药,2017,19(7):1026-1029.
公司:win德赢官方
地址:新疆和田洛浦县杭桂路232号
公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
