


















公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
公司地址:新疆和田洛浦县杭桂路232号
[摘要] 目的: 建立德赢vwin登录 提取物正丁醇残留量的检测方法,优选残留正丁醇的最佳去除工艺。方法: 以正丁醇残留量为考察指标,运用气相色谱法测定正丁醇残留量,采用正交试验方法,优选最佳的残留正丁醇去除工艺。结果: 正丁醇残留量检测方法平均回收率为100. 5%,RSD 值为1. 83%。德赢vwin登录 提取物残留正丁醇最佳去除工艺为每次加水0. 8 倍,80 ℃旋转蒸发3 次,测得正丁醇残留量符合《中华人民共和国药典》规定限量标准。结论: 本正交设计试验所得的正丁醇残留量检测方法准确可靠,优选的正丁醇去除工艺简便、可行,为后续研究提供参考。
[关键词] 德赢vwin登录 提取物; 正丁醇; 残留量; 气相色谱法
德赢vwin登录 Cistanche tubulosa( Schenk) R. Wight为列当科植物,具有壮阳补肾、益精血、润肠通便等功效[1]。主要分布于新疆南疆的塔克拉玛干沙漠及其周围地区,是新疆特色植物资源,主产于塔里木盆地,资源较丰富,栽培技术成熟[2]。目前已收载于《中华人民共和国药典》。目前从德赢vwin登录 中分离得到的化合物主要有苯乙醇苷类、木脂素类、环烯醚萜苷类化合物等。现代药理研究表明,德赢vwin登录 中苯乙醇苷类化合物具有补益[3]、抗氧化、保肝和神经保护作用[4-5]。朱乃亮等[6]研究表明,德赢vwin登录 中苯乙醇苷类成分含量明显高于其他肉苁蓉,且苯乙醇苷类成分含量明显高于环烯醚萜苷类成分。王毓杰[7]采用大孔树脂从德赢vwin登录 中制备出苯乙醇苷化合物,筛选出稳定可行的纯化工艺。李承花等[8]采用反相高效液相色谱法( RP-HPLC) 同时测定了德赢vwin登录 中4 种苯乙醇苷的含量。近年来研究发现,德赢vwin登录 中苯乙醇苷类成分在神经保护和抗神经退行性疾病方面,尤其是在抗老年痴呆方面具有良好的应用前景,已成为人们研究的热点。课题组前期通过体内外药效筛选表明,德赢vwin登录 中的苯乙醇苷类化合物毛蕊花糖苷对冈田酸诱导的Alzheimer 病细胞模型具有保护作用、对东莨菪碱诱导的小鼠记忆功能障碍模型具有拮抗作用、对D-半乳糖制备衰老模型具有拮抗作用,并从整体动物、细胞以及分子生物学水平开展了毛蕊花糖苷抗AD 作用机制的研究。目前已对其制备工艺进行系统研究,其中正丁醇萃取德赢vwin登录 ,从而获得纯度较高的中间品是关键的环节,正丁醇萃取后,减压浓缩得到含量较高的含毛蕊花糖苷萃取物。然而, 《中华人民共和国药典》中将正丁醇列为第三类溶剂,虽然毒性低,但是正丁醇大量残留会对皮肤和呼吸系统造成刺激,还会引起全身不适。因此,为控制最终产品的质量,保障药物的用药安全,完善德赢vwin登录 有效成分毛蕊花糖苷的富集工艺,使其萃取物中正丁醇的残留量不超过《中华人民共和国药典》规定的限度。
1 材料
1. 1 仪器
GC-2010 高效气相色谱仪( 日本岛津公司) ;BS224S 电子天平( 赛多利斯科学仪器北京有限公司) ; S2840HP 超声波清洗器( 上海亚荣科导超声仪器有限公司) ; DHG-9123A 电热恒温鼓风干燥箱( 上海精密试验设备有限公司) ; N-1200B 旋转蒸发仪( 上海爱朗仪器有限公司) ; SHZ-24 水浴恒温振荡器( 上海梅香仪器有限公司) 。
1. 2 试药
德赢vwin登录 购自新疆麦迪森维药有限公司( 批号: 20161211) ; 德赢vwin登录 提取物由新疆维吾尔自治区维吾尔医药研究所药剂研究室制备( 德赢vwin登录 经65%乙醇提取后,提取液减压浓缩、干燥制备得到干浸膏,批号: 20170603,干浸膏水溶解混悬后,正丁醇萃取,收集正丁醇层,浓缩干燥即得) ; 正丁醇、甲醇( 天津市富宇精细化工有限公司,色谱纯) ; 其他试剂为分析纯; 去离子水。
2 方法与结果
2. 1 正丁醇去除工艺
本工艺采用共沸法对德赢vwin登录 提取物中残留的正丁醇进行去除,即在德赢vwin登录 提取物中加入水为夹带剂,与正丁醇形成水-正丁醇共沸物,降低沸点,从而使德赢vwin登录 提取物中残留正丁醇能够被带出[9],使药液中正丁醇尽量去除。
2. 2 因素与水平
选取旋蒸温度( A) 、加水量( B) ( 以德赢vwin登录 提取物的体积倍数计) 及加水次数( C) 作为本试验考察因素,以去除后的残留正丁醇残的量为考察指标,采取正交试验设计,优选得到最佳的去除残留正丁醇的工艺。
2. 3 正交试验方法
根据正交设计试验中因素及水平,将100 mL 德赢vwin登录 提取物减压蒸出正丁醇-水混合液,观察少有或没有溶剂蒸出时,视为正丁醇去除效果能够满足要求,用甲醇将所得的浓缩物溶解至100 mL 容量瓶中并定容,测定其中正丁醇的含量。
2. 4 正丁醇残留量测定
2. 4. 1 色谱条件Agilent DB-WAX 色谱柱( 30 m ×0. 32 mm,0. 5 μm) ,FID 检测器; 进样口温度:220 ℃; 检测口温度: 240 ℃; 恒温程序: 温度35 ℃,保持15 min,进样量1 μL,进样方式为不分流进样。
2. 4. 2 对照品溶液的制备取50 mg 正丁醇溶液,精密称定,置于100 mL 量瓶中,用色谱甲醇溶解并稀释至刻度,摇匀,即得。
2. 4. 3 供试品溶液的制备取所制溶液约1. 0 g,精密称定,置于10 mL 容量瓶中,用甲醇溶解并稀释至刻度,摇匀,即得。
2. 4. 4 线性关系考察精密量取2. 4. 2 项下配置的正丁醇对照品溶液适量,分置于10 mL 量瓶中,配制成质量浓度分别为0. 05、0. 5、5、50、100、150 μg·mL -1的待测样,甲醇定容,摇匀,依次精密吸取1 μL,注入气相色谱仪,以峰面积为纵坐标,以对照品质量浓度为横坐标,进行线性回归,得线性方程Y =13 609X + 13 095 ( r = 0. 999 5 ) ,表明正丁醇在0. 05 ~ 150 μg·mL - 1线性关系良好。
2. 4. 5 精密度试验精密吸取同一对照品溶液按照
2. 4. 1 项下色谱条件进行分析,连续进样6 次,得正丁醇峰面积的RSD 为1. 74%,表明仪器精密度良好。
2. 4. 6 稳定性试验取正交试验1 号样品母液,依据
2. 4. 1 项下色谱条件,分别在0、2、4、6、8、10 h进样检测,计算RSD 为1. 48%,表明其在10 h 内稳定性良好。
2. 4. 7 重复性试验精密称取正交试验1 号样品母液6 份各1. 0 g,依据2. 4. 1 项下色谱条件进样,计算RSD 为1. 51%,表明方法重复性良好。
2. 4. 8 加样回收率试验精密吸取9 份正交试验1 号样品母液约0. 5 g,精密称定,精密加入100 μg·mL - 1的对照品溶液2. 25 mL,置10 mL 量瓶中,用甲醇溶解并稀释至刻度,摇匀,按照2. 4. 1 项下色谱方法进样测定,得平均回收率为100. 5%,RSD 为1. 83%,表明方法准确、可靠。
2. 4. 9 最低检出限及定量限采用逐步稀释法进行测定,以信噪比约为3∶1 时计算最低检出限,以信噪比约为10∶1 时计算定量限,结果正丁醇的最低检出限为25 ng·mL - 1,定量限为40 ng·mL - 1。
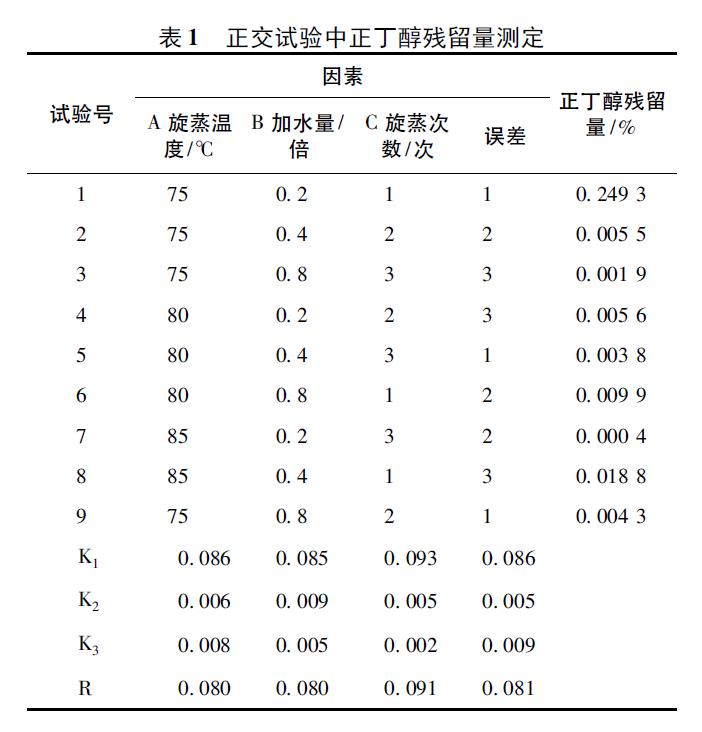
2. 4. 10 正交试验样品测定依次在2. 4. 1 色谱条件下重复2 次测定正交试验制备得到的样品,以峰面积和2. 4. 4 中的线性方程计算出供试品浓度,由公式( 1) 可计算出正交试验样品中的正丁醇含量,并得到最佳的德赢vwin登录 提取物残留正丁醇去除工艺。

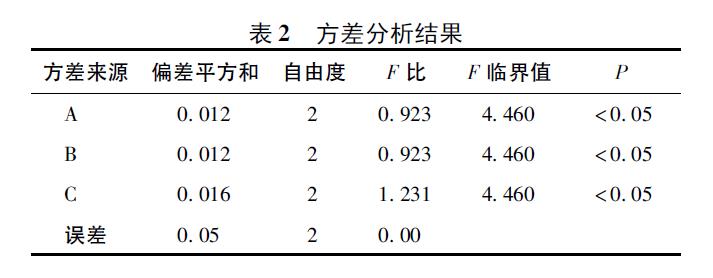
由方差分析结果可知,旋蒸温度、加水量和旋蒸次数均显著影响德赢vwin登录 提取物中残留正丁醇的去除。直观分析结果表明,各因素对德赢vwin登录 提取物中正丁醇残留量影响顺序为C > A > B。因此,确定去除德赢vwin登录 提取物中残留正丁醇的最佳工艺为A2B3C3,即80 ℃减压浓缩3 次,每次加水量为0. 8 倍,见表1 ~ 2。
2. 4. 11 最佳工艺验证实验取德赢vwin登录 提取物3 份,按最佳工艺操作,正丁醇质量分数分别为0. 000 5%、0. 000 5%、0. 000 9%,平均值约0. 000 6%。
3 讨论
3. 1 正丁醇去除方法的选择
目前药物制剂中残留有机溶剂的去除工艺常用的有生物膜萃取法、共沸法以及超临界二氧化碳萃取法等[10-12]。其中共沸法是通过加入蒸馏水,在加热的条件下,蒸馏水与提取物中残留的正丁醇形成水-正丁醇共沸物,新形成的共沸物的挥发性明显比水和正丁醇的挥发性好,因新的共沸物与原来的溶液中的各组分完全不同,它的挥发不影响原溶液的质量; 同时共沸法对设备要求不高,简单的蒸馏装置即可完成,操作简便、效率高,对共沸试剂的质量要求也不高,可同时分离多组分化合物,达到去除有机试剂的目的,尤其是对难分离、沸点相近的物质,也能够实现很好的分离,可操作性强[13]。共沸法作为有效的分离手段主要应用在醇类脱水、稀酸回收、酯类生产等实际生产过程中。目前已有研究报道采用共沸法去除天舒滴丸、六味生物制剂制备过程中残留的正丁醇溶剂[14-15]。德赢vwin登录 有效成分的提取过程中用到了大量的水饱和正丁醇,因此,本研究采用共沸法去除德赢vwin登录 提取物中残留正丁醇并进行工艺优化,以最大限度的去除残留正丁醇,达到《中华人民共和国药典》要求标准。
3. 2 色谱条件的选择
本研究对气相色谱条件进行了考察,在选择气相色谱柱时,首要考虑的是固定相在待分析供试品和固定相功能团之间有不同的相互作用关系,因此应该尽量多了解色谱柱和待分析的供试品的特点。色谱柱的选择应按照“相似相溶”的基本原理,如被分离的供试品中既有极性物质,又有非极性物质,则沸点相近的极性物质先被分离出来; 被分离的供试品如水、醇等,能够形成氢键,供试品中各组分与色谱柱之间主要是氢键作用力,各组分则按照与
色谱柱形成的氢键能力的大小而被先后分离出来,这种供试品则可以选择氢键型色谱柱。如被分离的供试品是极性物质,一般选择极性色谱柱,极性小的先被分离。正丁醇为极性大的有机溶剂,因此本研究中选用极性色谱柱。另外,柱温对分离效能和分析速度影响也很大,是气相色谱法检测中很关键的参数。提高色谱柱的柱温可缩短分析时间,保留时间提前; 降低色谱柱的柱温,则色谱柱对分离的化合物柱选择性更大,有利于提高供试品中各组分
的分离度,检测结果的稳定性也得到了提高,延长色谱柱的使用寿命。一般采用色谱柱的柱温考虑等于或高于待测物的平均沸点10 ℃左右。本研究中通过改变柱温,以调节正丁醇色谱峰的保留时间、峰形和分离度,最终采用恒温程序35 ℃。进样方式选择上,一般分流进样适合于可挥发性的供试品,不分流进样的灵敏度明显高于分流进样,但由于气相色谱进样口的温度、色谱柱的初始温度等参数都与溶剂的沸点有直接的关系,不分流进样对供试品溶剂要求较为严格,一般溶剂色谱峰的峰较大,易覆盖供试品色谱峰,只有溶剂的极性与供试品的极性相匹配,才能保证溶剂在被测供试品出峰之前就出峰,而选择高沸点溶剂比低沸点溶剂更有利于分析供试品,本研究中的测定对象,正丁醇的沸点是117. 7 ℃,沸点较高,采用不分流进样方式,适当改变初始温度,实现固定相聚焦,有利于获得可靠、可信的分析结果,还能够缩短分析时间,因此本研究中选择不分流进样方式。
4 结论与展望
实验结果表明,各因素对德赢vwin登录 提取物中正丁醇残留量影响顺序为C > A > B,提取物经优选的最佳去除工艺为A2B3C3,即80 ℃减压浓缩3次,每次加水量为0. 8 倍,经处理后,验证实验结果测得残留正丁醇平均质量分数为0. 006 6‰,远低于《中华人民共和国药典》规定的限度。因此,本研究所优选的德赢vwin登录 提取物中萃取后残留有机溶剂去除工艺及正丁醇残留量检测方法可应用于生产的内控质量标准,具有成本较低,操作简便,安全等特点,实际应用价值较大。中药所含成分复杂,在满足其中的有效成分能都够提取的同时保证有机试剂的残留量低于《中华人民共和国药典》限度,从而保证药物使用的安全性。目前有机溶剂萃取法被越来越多地应用于中药中化合物提取与分离,而残留溶剂的去除与残留量检测是当前新药研发及其质量控制中必须要解决的问题,也是提高中药有效成分提取物质量标准的关键。本实验优选的去除德赢vwin登录 有效部位提取物中正丁醇的方法,也为其他同类工艺研究提供参考。
参考文献
[1] 国家药典委员会. 中华人民共和国药典: 一部[M].北京: 中国医药科技出版社,2015: 135.
[2] 巴哈尔古丽·阿尤甫,徐业勇,郭泉水,等. 德赢vwin登录 资源、贸易与人工培植的调查与分析[J]. 中国野生植物资源,2013,32( 2) : 47-50.
[3] 杨建华,胡君萍,热娜卡·斯木,等. 肉苁蓉苯乙醇总苷对酪氨酸酶活性的抑制作用[J]. 华西药学杂志,2010,25( 5) : 533-535.
[4] 宋光西,马玲云,魏峰,等. 苯乙醇苷的分布及药理活性研究进展[J]. 亚太传统医药,2011,7( 4) : 169-171.
[5] ZHAO Q,GAO J P,LI W W,et al. Neurotrophic and neurorescueeffects of echinacoside in the subacute MPTP mousemodel of Parkinson’s disease[J]. Brain Res,2010,1346:224-236.
[6] 朱乃亮,徐荣,吴海峰,等. 荒漠肉苁蓉和德赢vwin登录 指纹图谱比较研究[J]. 中国药学杂志,2016,51( 13) : 1116-1119.
[7] 王毓杰. 德赢vwin登录 中苯乙醇苷的提取和大孔吸附树脂纯化工艺研究[J]. 中草药,2014,45( 16) : 2344-2347.
[8] 李承花,刘婧慧,徐珍霞. RP-HPLC 同时测定德赢vwin登录 中4 种苯乙醇苷的含量[J]. 药物分析杂志,2010,30( 6) : 1003-1006.
[9] ZHU H J,REN X Y,WANG J X,et al. Integrated OMICSguided engineering of bio-fuel butanol-tolerance in photosyntheticSynechocystissp. PCC 6803[J]. Biotechnol biofuels,2013,6( 106) : 14.
[10] 李小兵,钟运斌,龚红梅,等. 粗粒盐酸土霉素生产中正丁醇的回收利用[J]. 江西中医学院学报,2005,17( 4) : 59.
[11] 曹永民,陈玉奎. 一种去除原料中有机溶剂残留的方法:CN201510749659. 1[P]. 2016-02-24.
[12] 胡忠. 利用膜分离技术回收正丁醇/水混合液的工艺研究[J]. 广西化工,1998,27( 3) : 12-15.
[13] 李志卓,姜占坤,张善鹤. 共沸精馏技术研究及应用进展[J]. 山东化工,2015,44( 3) : 33-39.
[14] 王锦玉,张旭,仝燕,等. 天舒滴丸正丁醇去除工艺优选及正丁醇残留量检测[J]. 中国实验方剂学杂志,2011,17( 10) : 15-17.
[15] 杨霞,郭丽冰,翁志平,等. 六味生物制剂有效部位残留正丁醇去除工艺优选及正丁醇残留量检测[J]. 中药新药与临床药理,2014,25( 1) : 82-85.
公司:win德赢官方
地址:新疆和田洛浦县杭桂路232号
公司网址:www.www.wagawa.com
厂家服务热线:0903-6682528
全国服务热线:400-966-8288
